A perfect match: cuando la física y la medicina se encuentran
Publicado el 8 de marzo de 2026
Jimena Miguel Serna


Ilustración de Jimena Miguel Serna
La Dra. Marina García Cardosa encuentra especial interés en la unión entre la física y la medicina. Recién doctorada por la Universidad de Navarra en Física Médica, ha orientado su trabajo, desde la ingeniería, hacia un objetivo muy concreto: que el conocimiento sirva para mejorar y ayudar a la sociedad.
Esa búsqueda de impacto la llevó a mirar hacia la física médica, un terreno donde la investigación se conecta directamente con el paciente.
Ha obtenido el premio a la mejor tesis doctoral de Física Médica de la Real Sociedad Española de Física por su investigación.

La Dra. Marina García Cardosa fotografiada en la entrada del Edificio de Ciencias de la Universidad de Navarra, sosteniendo el manuscrito de su tesis doctoral.
¿Por qué decidió realizar la tesis aquí y en este campo?
En primer lugar, por el campo. Yo quería hacerlo enfocado en mecánica de fluidos con aplicación médica. Estudié Ingeniería porque disfrutaba resolviendo problemas de física o matemáticas y buscaba algo dinámico, cambiante, pero sobre todo quería que mi investigación tuviera un impacto real; en este caso, en la medicina. Por eso terminé contactando con la Universidad de Navarra al terminar mis estudios en Málaga. Me propusieron varias líneas de investigación y una de ellas es mi tesis: el desarrollo de un modelo que determine de manera personalizada la radiación que recibe la sangre durante los tratamientos de radioterapia. Estoy muy agradecida a la Asociación de Amigos, que me concedieron la beca para hacer el doctorado.
¿Cuál fue la novedad en la tesis con respecto a la carrera?
Tener tiempo real para aprender. En el grado todo iba muy rápido, tenía una serie de asignaturas y muchas veces no podía dedicar el tiempo que hubiese deseado para entender completamente el tema. Sin embargo, en la tesis podía pararme, revisar conceptos y dedicarle a cada parte el tiempo que fuera necesario. Por ejemplo, si sabía que tres conceptos me ayudarían a avanzar, podía invertir días en comprenderlo bien. Fue un cambio en la forma de trabajo; ya no era aprobar una asignatura, sino que podía detenerme y construir conocimiento con calma. Aunque tienes otro tipo de presión y exigencias, disminuye la presión de aprender a tiempo para los exámenes.
Su tesis investiga cómo la radioterapia daña la sangre. ¿Podría profundizar más?
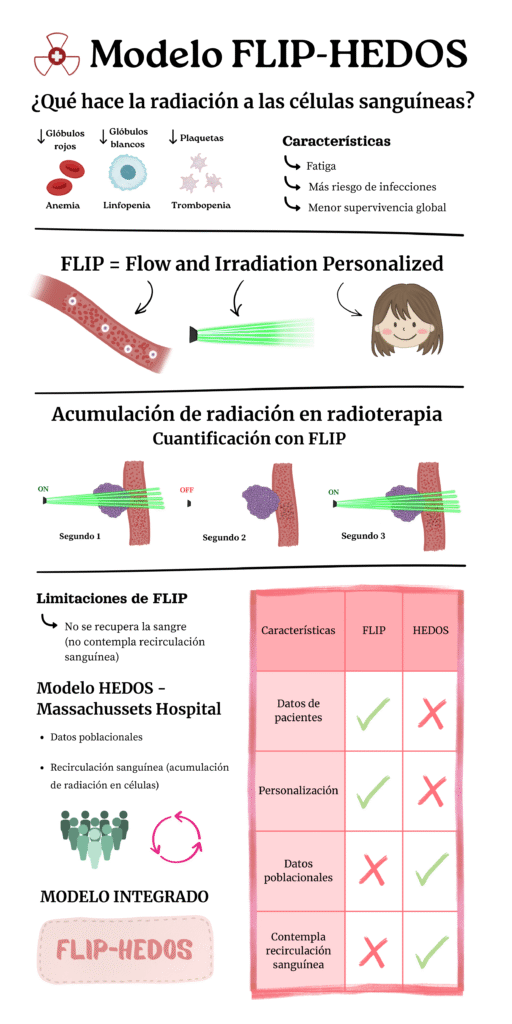
La radiación ionizante es utilizada en oncología radioterápica debido a su capacidad para dañar el ADN, por lo que se aprovecha para el control tumoral. Sin embargo, hay un área poco estudiada: el daño a la sangre circulante provocado por la radiación. Esto se traduce en anemia, afecciones en el sistema inmunológico (mayor riesgo de infecciones en pacientes inmunodeprimidos) y fatiga persistente, que reduce la media de supervivencia de los pacientes. Sabíamos que la radiación provoca estos daños a la sangre, pero su estudio se ha visto limitado por su enorme complejidad: no es posible caracterizar al completo y con precisión la hemodinámica de un paciente. No obstante, a partir de 2020, empiezan a desarrollarse modelos para ello que tienen como objetivo el determinar la dosis sanguínea durante tratamientos de radioterapia.
Lo que diferencia el enfoque de mi tesis del resto de modelos que buscan predecir este daño es que se utilizan los datos del paciente específico que se va a tratar. La mayoría de los modelos existentes hacen uso de datos poblacionales o genéricos. Durante mi tesis, hemos desarrollado el método FLIP (Flow and Irradiation Personalized), una metodología que permite determinar la dosis que recibe la sangre de un paciente específico durante su tratamiento de radioterapia. El flow del FLIP se refiere a la geometría de los vasos sanguíneos junto con la velocidad a la que viaja la sangre, el flujo; el irradiation hace referencia al momento en que la radiación es enviada, es decir, discierne entre encendido y apagado del haz de fotones o protones. Esta metodología calcula la radiación que recibe cada elemento sanguíneo, lo cual se mide en Gy. Por ejemplo, en el segundo 1 recibe 0,01 Gy, en el segundo 2, nada y en el segundo 4 vuelve a recibir 0,01 Gy y se acumula radiación.
Sin embargo, nuestro método no tenía en cuenta que ese elemento sanguíneo pudiese volver a visitar ese vaso sanguíneo. Como tenía sus limitaciones, me fui de estancia al Massachusetts General Hospital para introducir nuestra metodología en su herramienta, HEDOS, de tal forma que ambos modelos se complementaran, pues esta segunda utilizaba datos poblacionales.
Infografía de Jimena Miguel Serna
¿A qué resultados se llegaron?
Observamos que el tamaño del tumor y la cercanía con los vasos sanguíneos son factores determinantes, pues en estos casos la sangre recibe una mayor dosis de radiación y en algunos casos es imposible que las células sanguíneas lleguen a recibir algo, pero sí se pueden plantear estrategias de mejora e incluso dar apoyo a la toma de ciertas decisiones. Además, nuestro modelo tenía una ventaja y es que combinamos los datos de pacientes reales con las medias poblacionales de pacientes de cáncer (FLIP-HEDOS), lo que resulta muy útil para cuantificar la radiación recibida por la sangre.
¿Cuáles fueron los principales retos de la investigación?
Utilizar datos de pacientes porque no son ideales; son difíciles de procesar. Cada paciente es único, lo que es maravilloso, pero también complejo. Por eso, han sido datos de 10 pacientes y no de 50, dado que trabajar con cada paciente requería mucho tiempo.
¿Cómo se aplicará su doctorado en medicina oncológica?
Mi objetivo es mejorar la herramienta de FLIP-HEDOS y que luego se use para ajustar el tratamiento de radioterapia. Primero debemos validar la herramienta, por ejemplo, realizando analíticas antes y tras el tratamiento (para medir la concentración de células sanguíneas). De esta manera podremos observar si los resultados obtenidos con el modelo son correctos. Después, hay que empezar a incorporarlo en tratamientos de radioterapia, para tratar a la sangre como un órgano de riesgo dinámico y ajustar las dosis y dirección de los haces de energía para minimizar su impacto. A largo plazo, ayudaría a personalizar aún más el tratamiento, especialmente en casos donde el tumor está cerca de grandes vasos sanguíneos, porque ahí es donde la recepción de radiación es prácticamente inevitable.
Ilustración de Jimena Miguel Serna
¿Ha habido algún momento durante la tesis que le haya hecho especial ilusión?
Cuando obtuve por primera vez resultados, invité a todos los compañeros y a mi director de tesis a desayunar. Fue un poco osado por mi parte porque no revisé si estaban bien o no, pero en ese momento tuve muchas ganas de celebrarlo.
¿En qué está trabajando actualmente?
Ahora mismo estoy de profesora de Bioestadística para el grado de Farmacia y de ayudante en otras asignaturas. Está siendo un curso intenso por la preparación de las clases y tampoco quiero dejar de lado la parte de investigación, donde continuamos con el desarrollo de FLIP-HEDOS, sobre el que ya hemos realizado una publicación. Queremos ampliar el estudio con más pacientes de la CUN y llegar a una muestra de 20 pacientes para poder tener conclusiones más clínicas.
Muchas gracias por mostrarnos que el objetivo no es solo curar, sino curar mejor.
La medicina es una disciplina cada vez más interdisciplinar y la física o la ingeniería tienen un enorme potencial a la hora de mejorar tratamientos médicos. Una mirada más precisa obliga a fijarse también en los efectos menos visibles.
En radioterapia, uno de los puntos ciegos era la sangre, pese a su papel esencial para la supervivencia del paciente. Investigaciones como la realizada por la Dra. Marina García Cardosa ponen el foco en un sistema dinámico que antes no era posible modelar para hacer cálculos con precisión.
