Tejiendo vida
Publicado el 30 de enero de 2026
Jimena Miguel Serna

Ilustración de Jimena Miguel
El infarto de miocardio es la primera causa de muerte en el mundo. Cada año, millones de personas sufren este evento cardiovascular y quienes sobreviven ven afectada gravemente su calidad de vida, pues el corazón no es capaz de reponerse.
Con esta premisa el Dr. Manuel Mazo quiso buscar una solución al problema. Él es el responsable del Grupo de investigación de Ingeniería de Tejidos Cardíaca del Cima Universidad de Navarra, que realiza impresiones 3D para poder implantar a pacientes que hayan sufrido un infarto. El proyecto, que se llama BRAVƎ, involucra a varios centros de investigación y el CIMA es el coordinador e ideador.
¿Cómo surgió la idea?
Fabricar tejido no es una idea nueva. Es una necesidad que existe desde siempre, por así decirlo; desde que existe el primer amputado surge esta idea de fabricar órganos. Las primeras prótesis estaban hechas de materiales naturales —como los piratas con su pata de palo, que es un ejemplo muy clásico— hasta que llegamos a los trasplantes en el siglo XX. Pero no es hasta que tenemos tecnologías mucho más avanzadas que se abre la posibilidad de de hacer órganos a demanda. Una de las formas de hacerlo es a través de células madre.
Con esta posibilidad de fabricar tejidos a demanda, la siguiente pregunta es inevitable: ¿en qué enfermedad tendría más impacto clínico? La necesidad detrás de la elección está en que las enfermedades cardiovasculares son la primera causa de muerte en el mundo, y esto ocurre porque el corazón no puede regenerarse.
Tú te haces una herida y sana; tienes una lesión muscular y se repara. Pero si tienes un problema cardíaco, como un infarto, este no se arregla, sino que debes vivir con él. A través de cambios en la alimentación o hábitos diarios puedes alargar tu esperanza de vida, pero al final la mitad de los pacientes llegan a un estado que se llama “fallo cardíaco”.
¿Cómo se consigue realizar? ¿Cuál es el proceso para llevarlo a cabo?
Para generar tejido cardíaco necesitamos tres componentes: las células, la matriz extracelular (el pegamento que mantiene unidas a las células) y la estructura tridimensional, porque todos los tejidos, excepto la piel, son en 3D. Para todos los componentes tenemos tecnologías que han sido facilitadoras o impulsadoras para su creación en laboratorio. Yo, por ejemplo, puedo hacerle un explante de su propia piel a una persona que ha tenido una quemadura grave. Esta crece en el laboratorio y genera un tejido bioartificial que se injerta al paciente. Sin embargo, muchos órganos no tienen una fuente celular. Se desarrollan en la fase embrionaria y en la etapa de crecimiento, pero en la edad adulta dejan de regenerarse. Los ejemplos más clásicos son el corazón y el sistema nervioso central. Para esto, las diferentes tecnologías de células madre han sido transformadoras.
Existen muchos tipos de células madre: las adultas son limitadas, las sanguíneas sirven para fabricar los distintos tipos de componentes de la sangre. Las que más capacidad tienen son las embrionarias, pero tienen una carga ética y legal que hace imposible trabajar con ellas.En 2006 se desarrolla una nueva tecnología que se llama reprogramación celular, que permite tomar una célula adulta y transformarla en una célula madre, como si hubiera sido tomada de un embrión. Se le conoce como célula madre humana pluripotente inducida, hiPSC (por sus siglas en inglés). Son las que nosotros utilizamos en este laboratorio para crear tejido cardíaco.
Por lo que, hasta este punto, ya tenemos la primera tecnología para fabricar uno de los componentes: en este caso, utilizamos las células madre para crear cardiomiocitos, células musculares de tipo cardíaco que se diferencian del músculo normal porque forman redes más complejas y que permiten que la contracción cardíaca sea muy eficiente. También debemos fabricar vasos sanguíneos porque el corazón tiene demanda metabólica y requerimos de fibroblastos para el estroma (que forma parte de la matriz extracelular y conecta los cardiomiocitos).
Igualmente, necesitamos matriz extracelular; ¿cómo la reemplazamos? Porque esto no son células; son moléculas como pueden ser el colágeno, el ácido hialurónico o la fibrina. Esto se consigue con biomateriales, que podemos encontrar también en cosméticos, por ejemplo. Actualmente, disponemos de materiales artificiales o semisintéticos, es decir, podemos crear materiales con propiedades a demanda; todo ello con limitaciones, claro.
El último pilar es la estructura tridimensional que se realiza fundamentalmente a través de tecnologías de fabricación aditiva; la más conocida, la impresión 3D. En este proceso, se diseña un objeto y, a través de diferentes métodos (el más común es el depósito organizado de un filamento), se crea un objeto 3D. Nosotros normalmente vemos piezas creadas con plástico, pero se puede aplicar esta tecnología al ámbito biológico y, en vez de fabricar un plástico, crear un tejido humano.
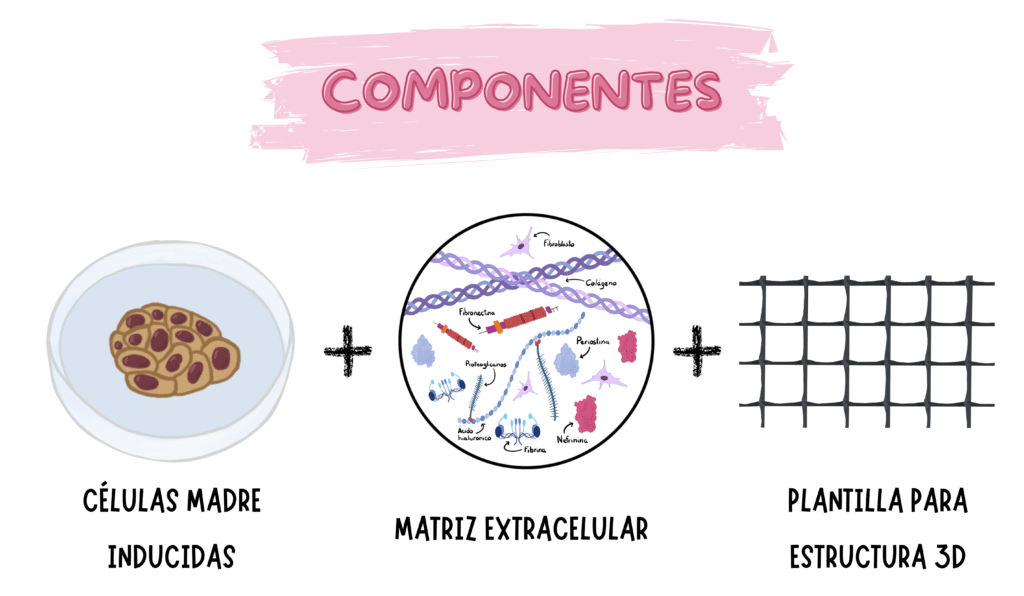
Ilustración de Jimena Miguel
Entonces, estas tres tecnologías se pueden aplicar a cualquier órgano que tenga necesidad de regeneración: un tabique nasal, un fragmento de hueso, el hígado o el páncreas. En nuestro caso, queremos fabricar tejido cardíaco, y una tecnología de impresión 3D altamente especializada es el Melt Electro-Writing. Se parece mucho a la técnica normal, pero, en lugar de fundir un plástico de espesor medio de 1 mm, es un filamento de 10 a 20 micras (0,01 mm). ¿Por qué hacemos esto? Porque si colocamos a la célula sobre un filamento demasiado grande, se percibirá como plano. En cambio, con Melt Electro-Writing imprimimos fibras muy finas y podemos dejar muchos huecos para que sean colonizados por células. Y según el diseño que creemos, vamos a determinar cómo se organizan las células para formar tejido.
Para el tejido cardíaco esto es fundamental. El corazón es el primer órgano que funciona en un embrión y el último en dejar de funcionar. ¿Cómo lo consigue? Porque es una estructura súper organizada. La contracción que produce una célula se suma a la contracción de la célula vecina. Si estuviesen dispuestas al azar, la contracción sería cero porque una célula “tira” hacia un lado y la siguiente hacia otro. Nosotros queremos imitar esta estructura tan perfecta.
Generamos un fragmento de tejido cardíaco, pero este presenta un problema, y es que es muy inmaduro. El músculo cardíaco es igual a los músculos normales en el sentido de que tiene que entrenarse. Nosotros comenzamos con un músculo primitivo y necesitamos entrenarlo. Esto es lo primero para que sea más potente y tenga más capacidad terapéutica.
¿Cómo se implanta en el paciente?
Actualmente solo lo hemos probado en modelos animales. Es necesario, antes de pasar a humanos, testear todos los tratamientos en animales, en este caso, ratones y cerdos, pues este último es el que tiene un corazón más similar al humano.
Nosotros modelamos el infarto imitando el proceso por el cual se produce. Un infarto ocurre cuando una de las arterias coronarias que riegan el corazón, se bloquea parcial o totalmente. Nosotros generamos este evento para que desarrolle el daño cardíaco, donde se observa una zona necrosada (muerte celular, una respuesta instantánea a la falta de irrigación sanguínea) y un aumento de cicatrización, así como una caída de la función cardíaca. Lo que se hace después es poner el tejido sobre el corazón del animal y evaluar cómo cambia la función, cómo se contrae el corazón. Esto se hace por ecocardiograma o resonancia magnética. Y, post mortem, también se evalúa cómo está ese tejido, si las células siguen ahí…
Hemos observado en estos ensayos preclínicos que los ratones trasplantados tienen una mejora muy importante de la contracción cardíaca y, en colaboración con el proyecto europeo BRAIN en la universidad de Lovaina, hemos hecho un estudio también en cerdos y conseguimos resultados muy prometedores. Estamos a las puertas de poder aplicarlo en humanos.
Entiendo que en este caso el rechazo por parte del sistema inmune no sería posible.
Sí que lo hay, pues no se trabaja con la células del propio paciente porque esto encarece mucho el proceso. El trasplante se realiza de una persona a otra. En el futuro, tal vez se podría trabajar con las propias células del paciente, pero lo alargaría mucho y, tal como nosotros trabajamos, no es viable actualmente. Pero sí cabe decir que estamos trabajando en estrategias que intenten rodear esa respuesta inmune para evitar el rechazo del trasplante.
¿Cómo se personaliza el tratamiento para cada sujeto?
De muchas formas. El corazón de cada persona es diferente: depende de su edad, costumbres deportivas, su género… El lugar en el que se tiene el infarto y la magnitud de este hará que la lesión sea diferente. Este es uno de los campos en los que más estamos trabajando. El último nivel de personalización sería utilizar las células del propio paciente, pero podría alargar el proceso entre 6 meses y un año.
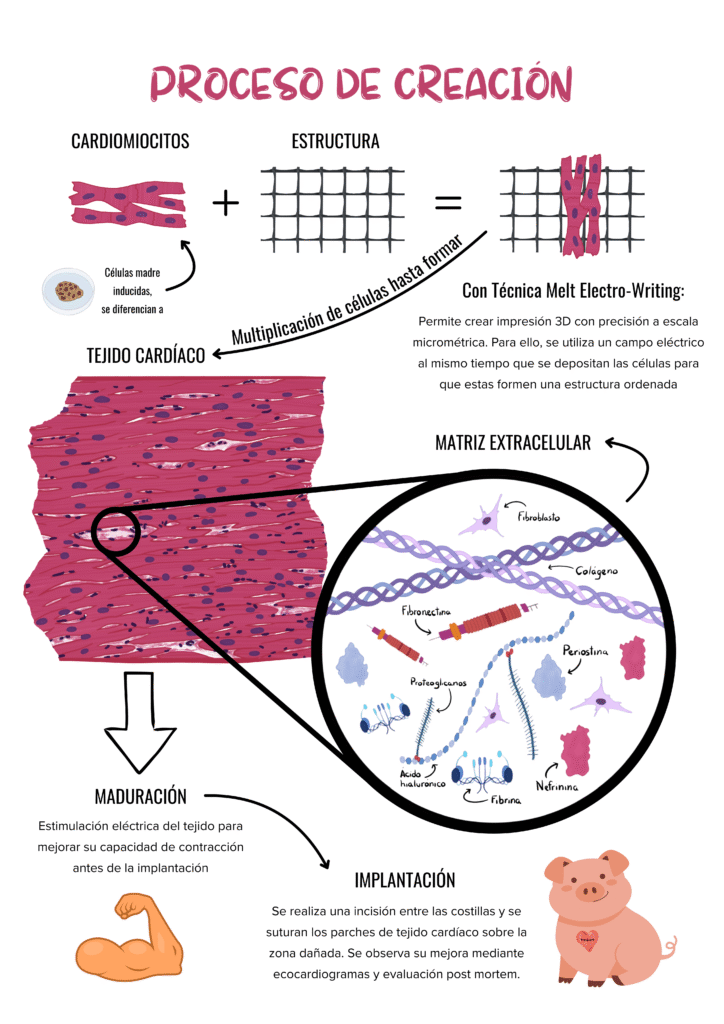
Ilustración de Jimena Miguel
¿Cuáles serían los pasos futuros para que este tratamiento pase a humanos y en unos años sea una realidad para los pacientes?
Primero deben producirse los tejidos bajo normas GMP (Good Manufacturing Practices) y validarse en estudios de seguridad. Luego se necesitará aprobación regulatoria y reducción de costes para iniciar ensayos clínicos. El paso inicial consiste en organizar el proceso de fabricación bajo condiciones regulatorias, es decir, garantizar que se realice en una sala estéril y con máquinas que tengan las garantías de seguridad y calidad. También se debe comprobar que en los ensayos con animales no haya componentes tóxicos en el tejido fabricado y que no se produzcan arritmias. Esperamos que la última fase, la de aprobación del ensayo, se alcance en un par de años. Estamos muy cerca y, aunque sabemos que nuestro tejido no será el definitivo, creemos que puede ser una opción muy viable para los pacientes.
También habría que plantear la producción a nivel logístico. Podemos producir de forma centralizada en un hospital o empresa, que fabrique y envíe los tejidos, o se puede pensar en una unidad de producción en cada hospital. En este punto, el reto principal es conseguir personal formado para dicha tarea. Dicho esto, creemos que estamos en un momento en el que tenemos un producto que puede ser terapéutico, pero, al mismo tiempo, tenemos un problema económico, ya que este tipo de terapias son muy caras. El proceso de generación de células cardíacas a partir de células madre tiene un coste de entre 50 y 100 euros por cada millón de células. En un infarto, el paciente puede necesitar entre 200 y 1000 millones de células, por lo que el coste sube mucho.
El resultado obtenido, ¿sería como el de un paciente “sano”, como si no hubiera tenido un infarto de miocardio?
¿Si revertiríamos la situación? No, tanto no; estamos hablando de daños muy grandes. Uno de los problemas de las terapias experimentales es que a los primeros pacientes a los que llega es a los más enfermos, por lo que es muy difícil obtener grandes resultados. Pero sí creemos que podemos mejorar la calidad de vida de muchas personas.
¿Se podría aplicar este tipo de terapias para otras enfermedades cardíacas?
Sí, el grupo trabaja también en crear válvulas 3D con componentes celulares, buscando que sean duraderas y eviten nuevas operaciones, especialmente en pacientes mayores.
En nuestro grupo trabajamos también para fabricar válvulas para aquellos que tengan deformidades, pero el estudio es todavía muy prematuro. Hemos puesto a punto procedimientos para obtener células específicas de esta estructura a partir de células madre pluripotentes. Ahora vamos a intentar crear válvulas 3D con estas células, que resultan útiles porque las válvulas actuales que se emplean son acelulares o mecánicas y se deben cambiar cada cierto tiempo. Las personas jóvenes no deberían tener ningún problema, pero con una edad avanzada resulta más difícil reponerse de la operación.
¿Qué siente al saber que su trabajo podría mejorar la calidad de vida de millones de personas?
Es un sueño hacer algo que sea útil. Por eso estamos aquí y no en otra investigación. A largo plazo, contribuiremos a la ciencia y solucionaremos una necesidad muy importante para la sociedad. Mi propósito es conseguir, entre toda la comunidad científica, un cambio.
¿Podría contar algún momento de la investigación que le haya hecho especial ilusión?
Pueden ser varios, como la primera vez que conseguí obtener células cardíacas a partir de células pluripotentes. Fue un subidón. Llamé corriendo a mi jefe para que lo viera. También cuando hicimos el primer estudio en animales. Recuerdo que estábamos volviendo de un congreso en Manchester y en el tren estaba con el ordenador haciendo la estadística, y ahí es donde salió que había un beneficio funcional.
Muchas gracias por permitirnos conocer su investigación. Nos ha demostrado que va mucho más allá de un simple trabajo de laboratorio; que busca realmente mejorar la vida de las personas.
La investigación liderada por el Dr. Mazo representa un paso esperanzador en la medicina regenerativa, al ofrecer una alternativa real para quienes han sufrido un infarto de miocardio. Los resultados obtenidos en modelos animales, con una mejora notable en la función cardíaca, demuestran el enorme potencial de esta línea de trabajo. Más allá de los avances tecnológicos, este proyecto refleja el compromiso de la ciencia. En definitiva, tejer vida es dar una segunda oportunidad a las personas, uniendo conocimiento y humanidad.
